2026年5月11日,国家药品监督管理局药品审评中心(CDE)发布了一份重磅文件——《间充质干细胞产品药学研究与评价技术指导原则(征求意见稿)》。
这是我国首次专门针对间充质干细胞(MSC)产品提出的系统性药学研究规范,涵盖从原材料、生产工艺、质量研究、稳定性到变更管理的全流程技术要求。
这份文件到底讲了什么?对行业意味着什么?本文为您逐一拆解。
一、文件背景与定位

原文链接https://www.cde.org.cn/main/news/viewInfoCommon/483c58e835b4072a9646021319acb2b9
5月11日,CDE正式发布该征求意见稿,共22页,向行业公开征求意见。这是继2017年《细胞治疗产品研究与评价技术指导原则(试行)》、2023年《人源干细胞产品药学研究与评价技术指导原则(试行)》、2026年1月《细胞治疗药品药学变更研究与评价技术指导原则(试行)》之后,首次专门针对间充质干细胞这一细分品类发布的药学技术指导文件。 其定位明确:适用于按照药品研发和申报路径的MSC产品上市申请阶段的药学研究与评价,主要关注注册上市申请(NDA)阶段的技术要求,以促进MSC产品的规范研究与创新发展。

二、适用范围:从“异体”出发,涵盖多种技术路线
指导原则的核心适用对象是异体MSC产品,同时对多种技术路线均作出明确纳入:

此外,指导原则还提及MSC来源的细胞外囊泡(EV)、PSC分化获得的神经细胞、胰岛细胞、心肌细胞、类器官、组织工程产品等细胞部分,“如适用也可适当参考”,体现了一定的前瞻性。

三、核心要点解读
1.生产用物料:从起始原材料到培养及辅料的全链条管控 (1)起始原材料管控 指导原则将起始原材料分为三类,分别提出不同要求:

**供者筛查:必须明确供者来源、健康状况、病史,病原微生物检测间隔建议不低于90天。供者筛选需具有策略性和前瞻性,考虑供者数量与产品产能的匹配。
**组织采集与运输:需建立质量管理体系,关注运输稳定性,入厂标准至少满足无菌、无支原体、低内毒素。
(2)培养基与辅料要求
❌ 尽量避免使用人/动物源血清;若必须使用,需做TSE/BSE风险评估和病毒检测。
❌ 禁用β-内酰胺类抗生素,其他抗生素也要严格控制。建议进行无抗生素替代工艺路线的开发。
✅ 辅料尽量选择风险低、级别高的产品。
指导原则建议使用无血清或成分限定培养基,减少动物来源成分的不确定性,提高产品一致性和安全性。

2.生产工艺:批次、工艺控制与细胞库三位一体
(1)批次与批量要求
原则上同一批次必须来自单一供者同一时期采集的组织。临床试验用药需符合GMP要求,并达到一定的批量以满足临床需求。
(2)工艺控制要求
明确关键工艺参数(时间、温度、pH、细胞密度、离心力等),鼓励避免在医疗机构对产品“再处理”。如必须,需签订质量协议并确保GMP环境。
(3)细胞库研究和检定要求
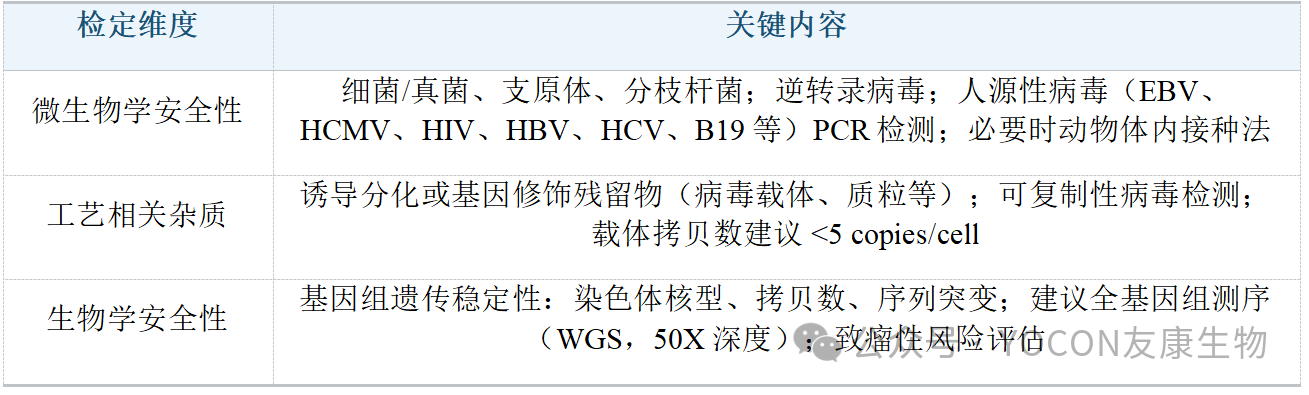
这是指导原则的重点内容之一。要求建立完善的细胞库分级体系(种子批→主细胞库→工作细胞库),检定聚焦三大安全性维度:
3.质量研究与质量标准:“功能标签”成为核心概念
“功能标签”是本指导原则提出的最重要核心概念,标志着MSC产品质量评价从“基本质控”向“疗效关联”升级。这一要求意味着,MSC药品不能仅仅停留在“细胞活率”“表面标志物阳性率”等基本质控指标上,而必须建立与产品临床适应症直接关联的效价评估体系。
定义:通过一系列体外或体内实验确定的、能够直接反映产品预期治疗作用(疗效)的、可定量测量的功能性指标或特征集合,是产品治疗效力的核心量化体现。 简单来说,就是用一组可量化的指标来证明“这批MSC药品确实有效”。不同功能定位MSC产品的功能标签示例:

其他关键质量要求见下表:
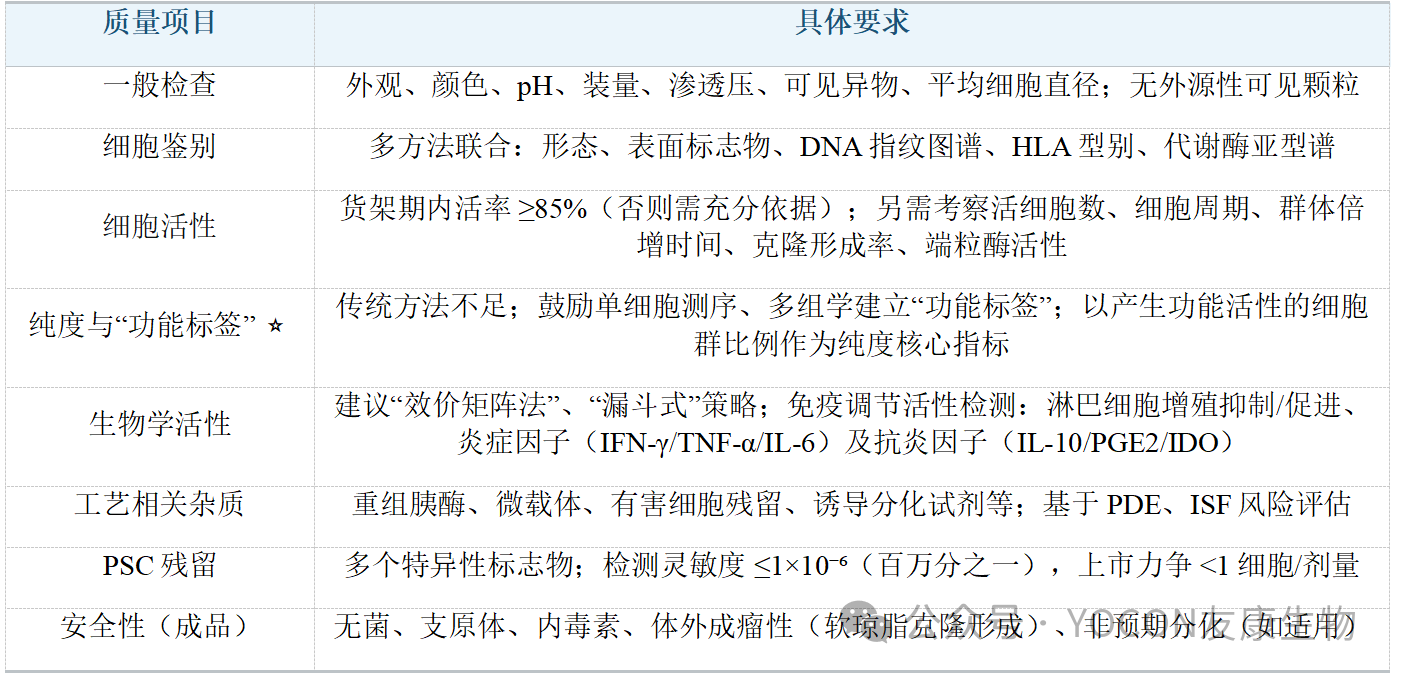
4.稳定性研究:全温度范围、多指标联动
需开展长期、加速、影响因素及临床使用中的稳定性研究,确保试验条件能代表临床实际情况。重点关注细胞活率、有效剂量和安全性指标,而非仅仅关注细胞活率。
这对细胞冻存液的性能提出了直接要求——冻存液的质量将直接影响MSC产品在冻存、复苏后的细胞活率、功能表型和效价保持情况。
5.变更研究与评价:明确红线,分级管理
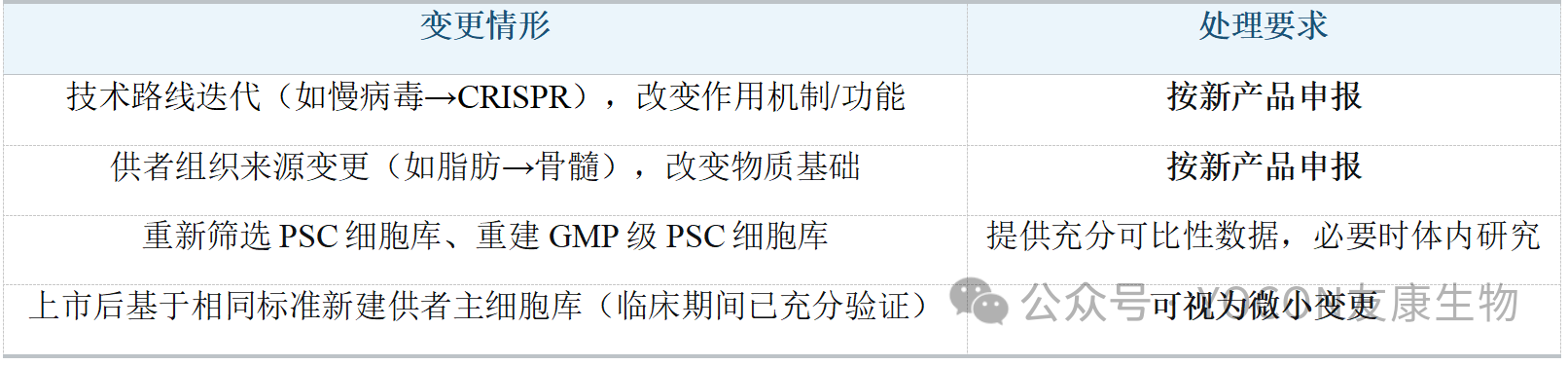
四、对行业的影响与启示
1.对MSC药品企业的影响 (1)药学研究标准全面提升。指导原则对MSC产品药学研究的要求远超此前的通用性指导,特别是在"功能标签"、细胞库检定、培养基与辅料控制等方面更加细化和严格。企业需要重新评估和完善现有的药学研究数据包。 (2)上市申报路径更加清晰。指导原则明确以NDA阶段的药学要求为核心,为企业规划上市申报提供了更明确的方向。 (3)变更管理有据可依。指导原则提出的变更分级管理思路,有助于企业在全生命周期中更好地规划和管理生产变更。 2.对上下游供应链的影响 指导原则对无血清培养基、成分限定培养基的推荐使用,将加速MSC药品企业从含血清培养基向无血清培养基的转型。同时,对细胞冻存液在稳定性研究中的重要性强调,也将推动GMP级细胞冻存液的市场需求。 此外,指导原则对功能标签检测、细胞表型分析等高端检测需求的提出,也将带动细胞治疗领域检测服务市场的发展。

GMP级间充质干细胞无血清培养基2.0
1无人源无动物源,所有蛋白均为人工重组,已获FDA DMF备案(31623),适用于临床。 2显著改善细胞贴壁与适应能力,兼备细胞高代次培养与外泌体收获。 3适配细胞工厂、微载体、生物反应器等2D及3D大规模培养模式。
1所有成分完全明确,无血清,无蛋白,无DMSO,已通过毒性实验和长期保存实验。
2采用复合式保护剂,显著降低冻存对细胞的损害,大幅提高细胞复苏率和活率。 3有明确申报案例,已关联药品进入中美双报临床Ⅱ期。友康可协助客户进行细胞药物申报中关于冻存液部分工作的指导。

友康无菌检测试剂盒系列
1快:2小时极速检测,终结周级等待。 2全:细菌/真菌/支原体三联检,一次核算提取同步完成三种微生物检测。 3灵:特异版(精准靶向药典菌)与广谱版(环境未知菌捕获)双模式灵活切换。 4合规:符合中美欧日药典(ChP/ USP/ EP/ JP),直通严苛监管市场。
YOCON
CDE本次发布的MSC药品征求意见稿,标志着国内MSC药品的监管要求正在从"通用性指导"向"品类专项指导"迈进。这既是对MSC药品研发的规范化要求,也是对行业发展的积极信号——更清晰的技术要求意味着更可预期的审评标准,有助于企业更好地规划研发和上市路径。

 友康生物
友康生物 2026-05-13
2026-05-13 行业热点
行业热点



